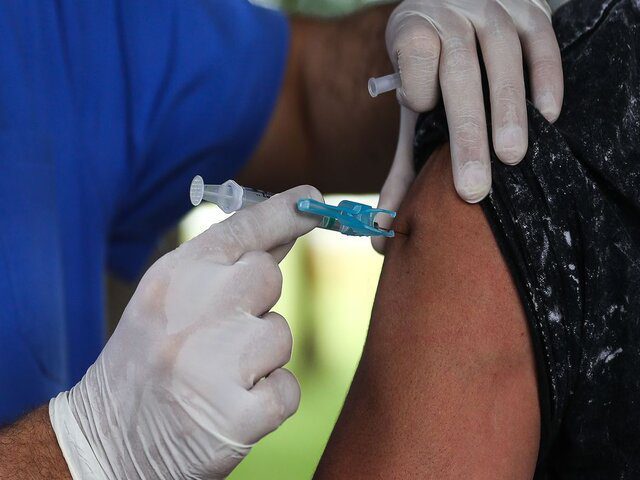
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta quinta-feira (16), o ensaio clínico Fase III da vacina quadrivalente (dividida e inativada) QIV-IB para Influenza, desenvolvida pelo Instituto Butantan. O estudo visa avaliar a imunogenicidade e a segurança da vacina em lactentes e crianças de seis a 35 meses.
O processo de produção da vacina quadrivalente é semelhante ao da vacina trivalente (dividida e inativada) do Instituto Butantan (TIV-IB) já utilizada em campanhas nacionais de vacinação contra Influenza.
Enquanto uma das vacinas trivalentes contém o vírus B (linhagem Yamagata – TIV-Y-IB) e a outra o vírus Influenza B (linhagem Victoria – TIV-V-IB), a vacina quadrivalente possui as duas cepas da linhagem B na mesma formulação.
Os ensaios clínicos são estudos de um novo medicamento conduzidos em seres humanos. A fase clínica visa demonstrar a segurança e a eficácia do medicamento experimental para a indicação proposta.
Caso seja comprovado que os benefícios superam os riscos, o medicamento experimental poderá ser registrado na Anvisa e disponibilizado no mercado brasileiro, desde que haja solicitação da empresa desenvolvedora/patrocinadora.